Organisation et division du noyau de la cellule
Organisation et division du noyau de la cellule
Les cellules vivantes ont une capacité remarquable à organiser leurs composants internes de manière précise et dynamique. Cela est particulièrement évident lors de la division cellulaire, où les cellules se réorganisent rapidement, dupliquent leur contenu et se divisent en deux cellules filles, qui adoptent souvent des destins distincts. Ces transformations complexes doivent être soigneusement coordonnées dans l’espace et le temps.
Notre laboratoire étudie les mécanismes moléculaires qui assurent cette coordination, à travers trois axes de recherche interconnectés :
Tout d’abord, nous étudions comment la ségrégation des chromosomes et la cytokinèse sont couplées, en particulier via le point de contrôle NoCut dépendant d’Aurora B, qui bloque l’abscission en présence de ponts chromatiniens. Ce projet, bien que toujours en cours, est en phase de finalisation.
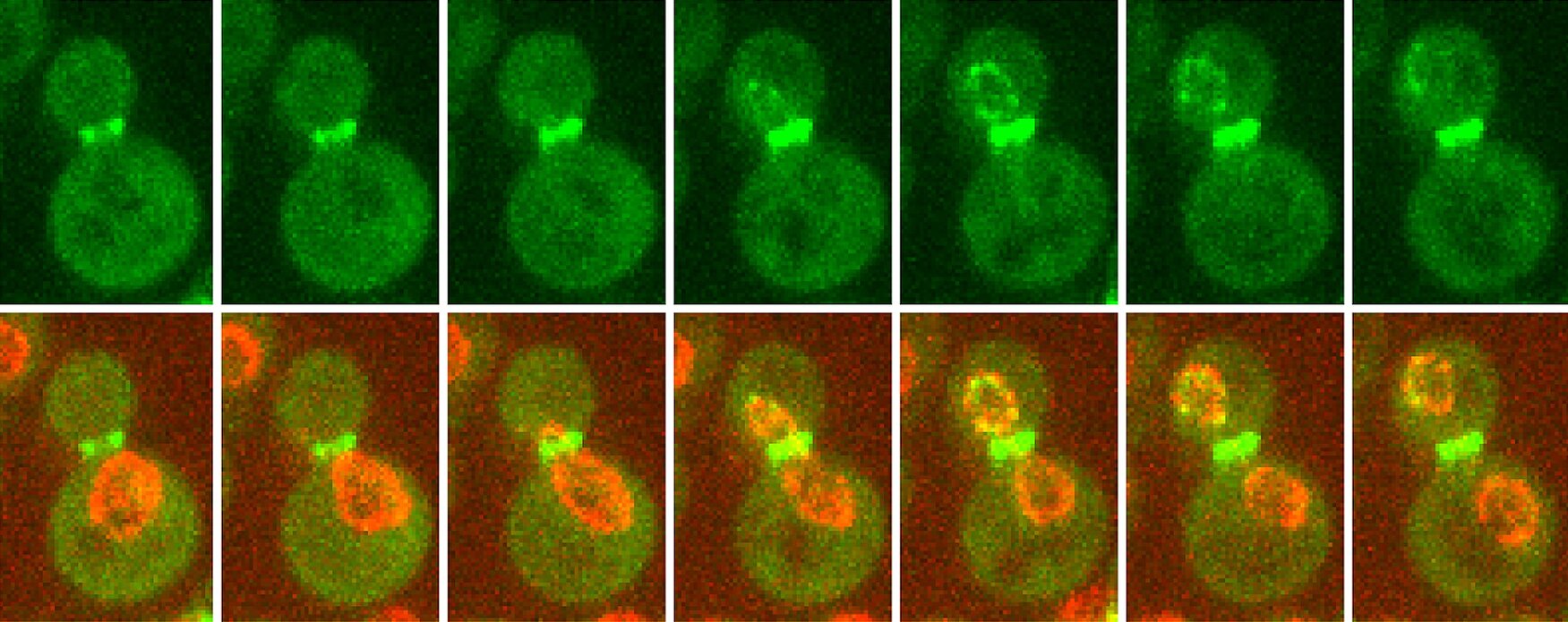
Ensuite, nous explorons comment l’organisation nucléaire influence l’identité cellulaire. Nous avons montré que les complexes des pores nucléaires (NPCs) sont acétylés différemment dans les cellules mères et filles chez la levure bourgeonnante, et que cette modification régule l’expression génique et l’export des ARNm. Nous cherchons à comprendre comment cette acétylation des NPCs module la transcription et les mécanismes post-transcriptionnels, et si des principes similaires s’appliquent chez les cellules souches embryonnaires (ES) de souris. Dans ce contexte, nous nous intéressons en particulier à l’impact de l’acétylation des protéines non-histones sur le traitement, l’export et la stabilité des ARNm au cours de la différenciation cellulaire.
Enfin, nous étudions comment les cellules maintiennent l’homéostasie nucléaire au cours du vieillissement. Chez la levure, des dommages à l’ADN ribosomique (rDNA) conduisent à la formation de cercles d’ADNr extra-chromosomiques (ERCs), qui s’accumulent dans les cellules mères âgées. Nous développons une approche protéomique basée sur le marquage de proximité pour identifier les protéines associées au rDNA lors de sa dégradation et de la formation d’ERCs. Ce projet, combinant spectrométrie de masse, imagerie en temps réel et microfluidique, vise à comprendre comment l’instabilité du rDNA perturbe l’organisation nucléaire et contribue au vieillissement cellulaire.
Ensemble, ces projets visent à comprendre comment les cellules préservent l’intégrité nucléaire et régulent l’expression génique via des réorganisations dynamiques de l’architecture nucléaire, avec des implications pour le développement et le vieillissement.
Membres
Chercheur(euse)s
Post-doctorant(e)s
Doctorant(e)s
Ingénieur(eure)s
Anciens membres
- Gabriel Neurohr (Group Leader at ETH Zurich)
- Iris Titos (Assistant Professor, Northwestern University, Chicago, Illinois, United States)
- Nuno Amaral (Technical Writer, Sweden)
- Aina Masgrau (Senior Validation Consultant, Spain)
- Andrea Battola (Medical Affairs Manager, Italy)
- Michael Maier (Postdoctoral Researcher, Institute of Medical Biology, Singapore)
- Francesca Di Giovanni (Technical Support Scientist, France)
- Tsvetomira Ivanova
- Arun Kumar (Postdoctoral Researcher, Cell and Molecular Biology Program, Pompeu Fabra University, Spain)
- Petra Stockinger (Research and Development Specialist, Spain)
- Zhanna Shcheprova (Senior Data Team Lead, France)
- Anne Daulny
- Trinidad Sanmartin (laboratory technician, Institute for Bioengineering of Catalonia, Spain)
- Mercè Gomar (Researcher Juan de la Cierva, University of Valencia, Spain)
- Céline Birling (ingénieur d'études, France)
- Vasilisa Pozharskaia (postdoctoral fellow in Université de Laval, Quebec City, Canada)
- Monica Dam (Research Scientist at Skyhawk Therapeutics, Basel, Switzerland)
Projets en cours
1. Contrôle du point de contrôle de la cytokinèse en réponse aux ponts chromatiniens
2. Régulation de l’expression génique et de l’export des ARNm par l’acétylation des pores nucléaires
3. Mécanismes de l’instabilité de l’ADN ribosomique et accumulation des cercles d’ADNr extra-chromosomiques au cours du vieillissement
Financements et partenaires
- Agence nationale de la recherche (ANR), coordinateur d'un projet de recherche collaborative, 2022-2025
- Fondation ARC pour la recherche sur le cancer, " Programme Labellisé ", 2022-2025
- Fondation pour la Recherche Médicale FRM, Equipe Labellisée, 2021-2024
Prix/Distinctions
European Research Council, Starting Grant (2011-2017)
Publications
2026
Article dans une revue
Roles of Srs2/PARI-family DNA helicases in NoCut checkpoint signaling and abscission regulation
- Monica Dam
- David F Moreno
- Nicola Brownlow
- Audrey Furst
- Coralie Spiegelhalter
- Manuel Mendoza
Journal of Cell Biology ; Volume: 224
2025
Article dans une revue
Chromatin Compaction Scaling with Cell Size Follows a Power Law from Interphase Through Mitosis
- Petra Stockinger
- Anna Oddone
- Melike Lakadamyali
- Manuel Mendoza
- Jérôme Solon
Biophysical Journal ; Volume: 124 ; Page: 3678-3689
Article dans une revue
Gene-specific transcript buffering revealed by perturbation of coactivator complexes
- Faezeh Forouzanfar
- David F Moreno
- Damien Plassard
- Audrey Furst
- Karen Amaral de Oliveira
- Bernardo Reina San Martin
- Làszlo Tora
- Nacho Molina
- Manuel Mendoza
Science Advances ; Volume: 11 ; Page: eadr1492
2024
Article dans une revue
Srs2/PARI DNA helicase mediates abscission inhibition in response to chromatin bridges in yeast and human cells
- Monica Dam
- Nicola Brownlow
- Audrey Furst
- Coralie Spiegelhalter
- Manuel Mendoza
BioRxiv
2022
Article dans une revue
Nuclear pore complex acetylation regulates mRNA export and cell cycle commitment in budding yeast
- Mercè Gomar-Alba
- Vasilisa Pozharskaia
- Bogdan Cichocki
- Celia Schaal
- Arun Kumar
- Basile Jacquel
- Gilles Charvin
- J Carlos Igual
- Manuel Mendoza
EMBO Journal
2021
Article dans une revue
Increased levels of mitochondrial import factor Mia40 prevent the aggregation of polyQ proteins in the cytosol
- Anna Schlagowski
- Katharina Knöringer
- Sandrine Morlot
- Ana Sánchez Vicente
- Tamara Flohr
- Lena Krämer
- Felix Boos
- Nabeel Khalid
- Sheraz Ahmed
- Jana Schramm
- Lena Murschall
- Per Haberkant
- Frank Stein
- Jan Riemer
- Benedikt Westermann
- Ralf Braun
- Konstanze Winklhofer
- Gilles Charvin
- Johannes Herrmann
EMBO Journal ; Volume: 40
2020
Article dans une revue
The budding yeast Start repressor Whi7 differs in regulation from Whi5, emerging as a major cell cycle brake in response to stress
- Ester Méndez
- Mercè Gomar-Alba
- M. Carmen Bañó
- Manuel Mendoza
- Inma Quilis
- J. Carlos Igual
Journal of Cell Science ; Volume: 133
Article dans une revue
Budding yeast complete DNA synthesis after chromosome segregation begins
- Tsvetomira Ivanova
- Michael Maier
- Alsu Missarova
- Céline Ziegler-Birling
- Monica Dam
- Mercè Gomar-Alba
- Lucas Carey
- Manuel Mendoza
Nature Communications ; Volume: 11
Article dans une revue
Impact of Chromosome Fusions on 3D Genome Organization and Gene Expression in Budding Yeast
- Marco Di Stefano
- Francesca Di Giovanni
- Vasilisa Pozharskaia
- Mercè Gomar-Alba
- Davide Baù
- Lucas Carey
- Marc Marti-Renom
- Manuel Mendoza
Genetics ; Volume: 214 ; Page: 651-667
Article dans une revue » Article de synthèse
Modulation of Cell Identity by Modification of Nuclear Pore Complexes
- Mercè Gomar-Alba
- Manuel Mendoza
Frontiers in Genetics ; Volume: 10 ; Page: 1301
Page 1 sur 3
