Cycle cellulaire et signalisation de l'ubiquitine
Cycle cellulaire et signalisation de l'ubiquitine
Le cycle cellulaire est un processus biologique fondamental qui assure le développement de l'organisme et sa dérégulation est liée à de nombreuses maladies humaines. La bonne exécution de la division cellulaire nécessite la duplication de tout le matériel génétique pendant la phase S, suivie de sa répartition précise entre deux cellules filles pendant la mitose. Au cours de ce processus, non seulement le matériel génétique, mais aussi les organites cellulaires doivent être répartis de manière égale dans les nouvelles cellules pour permettre leur bon fonctionnement. La machinerie du cycle cellulaire implique de nombreux facteurs et enzymes essentiels qui doivent être précisément régulés dans le temps et l'espace. Comment leur localisation correcte et au bon moment dans les compartiments subcellulaires est réalisée au cours des différentes transitions morphologiques du cycle cellulaire, reste une question importante dans le domaine.
L'un des mécanismes à l'origine de la fidélité de la division cellulaire est l'ubiquitylation (ou ubiquitination), qui est une modification covalente post-traductionnelle des substrats par une petite protéine, l'ubiquitine. L'ubiquitylation dirige fréquemment les substrats vers le protéasome 26S, qui sert de principal système pour la dégradation sélective des protéines. Cependant, l'ubiquitylation des protéines substrats peut également entraîner des événements non protéolytiques et jouer des fonctions importantes dans de nombreux processus cellulaires, y compris le cycle cellulaire. Notre groupe a décrit le rôle de la signalisation non-protéolytique de l'ubiquitine et la régulation des kinases essentielles pendant la mitose des cellules humaines. Cependant, on sait encore peu de choses sur la façon dont l'ubiquitylation de ces substrats essentiels détermine leur fonction et comment ces voies sont dérégulées dans les maladies humaines.
Grâce à notre expertise en biologie cellulaire, nous cherchons à découvrir de nouvelles voies qui régulent la répartition égale du matériel génétique et des organites cellulaires pendant la mitose et le réassemblage des pores nucléaires après l'achèvement de la division cellulaire. Nous souhaitons comprendre les mécanismes de régulation dépendants et indépendants de l'ubiquitine assurant la localisation des facteurs importants impliqués dans ces processus. En particulier, nous concentrons nos efforts actuels sur les protéines de liaison à l'ubiquitine (UBDs), qui interagissent avec les substrats ubiquitylés et médient leurs destins cellulaires et la signalisation en aval. Enfin, nous cherchons à identifier les liens possibles de ces voies avec des pathologies humaines telles que le cancer et les maladies neurologiques.

Membres
Chercheur(euse)s
Post-doctorant(e)s
Doctorant(e)s
Anciens membres
- Kyrylo Tron (University of Göttingen, Germany)
- Sadek Fournane
- Stephane Schmucker (University of Strasbourg)
- Paulo Costa (University of Strasbourg)
- Thibaud Metzger (Thermo Fisher Scientific
- Ksenia Krupina (UCSD, San Diego, USA)
- Katerina Jerabkova (University of Strasbourg)
- Sushil Awal (CRBM, Montpellier, France)
- Arantxa Agote Aran (ETH Zurich, Switzerland)
- Aurore Vuidel (Ksilink, Strasbourg, France)
- Inès Jmel Boyer (University of Dundee, UK)
Projets en cours
1. Le rôle de la protéine de liaison à l'ubiquitine UBASH3B dans la mitose et le cancer
Des anomalies au cours de la mitose provoquent l’aneuploïdie et la tétraploïdie des cellules, phénomènes récurrents dans la pathologie cancéreuse. La dérégulation des facteurs mitotiques est une caractéristique commune à de nombreux types de cancers. Par conséquent, les facteurs mitotiques constituent des cibles d’intérêt pour le développement de nouveaux agents thérapeutiques. Au cours de la mitose, l’attachement spécifique de molécules d’ubiquitine à des substrats protéiques régule des voies protéolytiques et non-protéolytiques. Les protéines de liaison à l’ubiquitine déterminent le devenir des substrats ubiquitinés et servent ainsi de récepteurs intracellulaires pour des signaux spécifiques dépendant de l’ubiquitine. Ces récepteurs de l’ubiquitine (Ub-récepteurs) représentent une nouvelle classe très attractive de cibles thérapeutiques. Cependant, à ce jour, aucune petite molécule inhibitrice de ces récepteurs n’a été développée pour un usage en thérapie anti-cancéreuse.
En collaboration avec la plateforme de criblage cellulaire à haut débit de l'IGBMC, nous avons réalisé un criblage visuel à haut débit de siARN en utilisant une bibliothèque humaine personnalisée de "décodeurs d'ubiquitine" et avons développé des protocoles de sélection de gènes basés sur des contrôles multiparamétriques. La liste des résultats contient de nombreuses nouvelles UBDs mitotiques. L'une des protéines UBD, UBASH3B, a déjà été caractérisée en détail dans notre laboratoire.
UBASH3B est le récepteur de la kinase mitotique Aurora B qui est essentielle pour la dynamique et la fidélité de la ségrégation chromosomique lors de la mitose. Au contraire de beaucoup d’autres Ub-récepteurs qui adressent leur substrat vers la dégradation protéique, UBASH3B ne régule pas le niveau protéique d’Aurora B. UBASH3B ne contrôle pas non plus l’activité enzymatique de la kinase. En revanche, UBASH3B se localise au fuseau mitotique où elle est essentielle au recrutement d’Aurora B sur les microtubules. Nos données récentes démontrent que la redistribution d’Aurora B des centromères vers les microtubules, médiée par UBASH3B, régule la dynamique et la fidélité de la ségrégation chromosomique et ainsi l’euploïdie des cellules.

Fig. 1. (A) Modèle de régulation de la localisation et de la fonction d'Aurora B par le récepteur d'ubiquitine UBASH3B. Aurora B (rouge) est ubiquitylée par CUL3 (bleu clair) et interagit avec UBASH3B (jaune) associé aux microtubules avant l'anaphase. UBASH3B est nécessaire et suffisant pour transférer Aurora B des régions centromériques des chromosomes (bleu) aux microtubules du fuseau mitotique (lignes noires), contrôlant ainsi ses fonctions centromériques et de kinétochores (gris) ainsi que le fuseau. UBASH3B agit de concert avec MKlp2 (vert) en ciblant Aurora B vers les futurs microtubules de la zone médiane et contrôle le timing et la fidélité de la ségrégation des chromosomes. (B) Modèle schématique décrivant un mode de régulation de la localisation d'Aurora B par UBASH3B et donc de la signalisation du point de contrôle de l'assemblage du fuseau (SAC). De faibles niveaux d’ UBASH3B induisent la propagation chromosomique d'Aurora B, l'activation du SAC et un arrêt mitotique persistant suivi d'une apoptose. Des niveaux élevés d’UBASH3B induisent une relocalisation prématurée d'Aurora B vers les microtubules, une inhibition du SAC et une aneuploïdie.
Nous pensons qu’UBASH3B représente un candidat idéal pour des thérapies anti-cancéreuses. Premièrement, malgré son expression ubiquitaire, des souris déficientes pour UBASH3B n’ont pas de phénotype notable. Deuxièmement, il a été montré que son niveau d’expression est augmenté dans des échantillons de patients atteints de cancers hautement agressifs. Troisièmement, dans des modèles animaux de cancer du sein, la surexpression d’UBASH3B favorise la présence de tumeurs invasives et de métastases. Enfin, nos résultats indiquent que la réduction du niveau d’UBASH3B par l’utilisation d’ARN interférents conduit à la mort cellulaire par apoptose dans des cellules issues de cancers agressifs.
UBASH3B représente donc une cible nouvelle et spécifique des cellules aneuploïdes de cancers dits agressifs. Sur la base de ces données, nous proposons qu’une perte de fonction d’UBASH3B dans les cellules cancéreuses conduira à leur mort par apoptose mais n’influencera que modérément les cellules primaires normales en division. En accord avec cet objectif, nous avons identifié un ensemble de petites molécules inhibitrices qui peuvent se lier spécifiquement à UBASH3B et l'inactiver pendant la mitose. Le traitement avec ces inhibiteurs entraîne l'arrêt mitotique et la mort spécifique des cellules cancéreuses mais pas des cellules primaires normales. L'objectif de ce projet de recherche est de valider les inhibiteurs d'UBASH3B comme composés anticancéreux principaux pour le développement de futurs médicaments. Les perspectives à long terme sont d'étendre cette stratégie à d'autres voies basées sur l'ubiquitine qui sont critiques pour la progression mitotique.
2. Régulation de l'assemblage des complexes de pores nucléaires
Les pores nucléaires (PN) constituent les seules portes de communication entre le noyau et le cytoplasme et assurent le fonctionnement et la survie de la cellule. Ils sont insérés dans l'enveloppe nucléaire (EN), une structure à double membrane qui entoure le noyau de la cellule et servent de médiateurs pour le transport et l'échange de protéines et d'ARN entre le noyau et le cytoplasme. Les nucléoporines (Nups) sont les unités protéiques constitutives des PN. Les Nups solubles existent dans le cytoplasme, mais la façon dont leur assemblage en PNs est limité à l’EN reste un mystère. Récemment, notre équipe a découvert que la famille des protéines apparentées à l'X fragile (FXRPs) (FXR1, FXR2 et FMRP) et le transport le long des microtubules dirigent l'assemblage spatial des Nups au niveau de l’EN dans les cellules humaines. En l'absence de FXRPs ou de microtubules, les Nups s'auto-assemblent de manière aberrante dans le cytoplasme en structures appelées granules de nucléoporines cytoplasmiques (GNC), et l'exportation des protéines et la progression du cycle cellulaire sont perturbées (Fig. 2). Il est important de noter que les modèles du syndrome de l'X fragile (SXF), où FMRP est absente, présentent des GNC, ce qui suggère que ces défauts peuvent contribuer à la pathologie du SXF. Le SXF est un syndrome neurodéveloppemental génétique rare et est la forme familiale la plus fréquente de déficience intellectuelle. Les patients atteints du SXF présentent également de nombreux problèmes de développement, y compris des comportements inappropriés, des malformations faciales et une macroorchidie. Actuellement, il n'existe aucun traitement curatif pour le SXF. L'objectif principal de ce projet de recherche est de comprendre si et comment les défauts dans l'homéostasie des Nups médient la pathologie du FXS. Nous émettons l'hypothèse que les dérégulations dans la voie des Nups peuvent perturber le développement neuronal par un ou plusieurs mécanismes possibles : inhibition du transport nucléocytoplasmique de protéines et/ou ARN spécifiques ou de facteurs nécessaires à la progression fidèle du cycle cellulaire en raison de leur séquestration dans les GNC et/ou perturbation des processus de traduction localisés des Nups. Cette recherche aidera probablement à comprendre comment une mauvaise régulation des Nups peut contribuer au SXF et pourrait créer de nouvelles perspectives thérapeutiques pour les patients atteints de cette maladie.
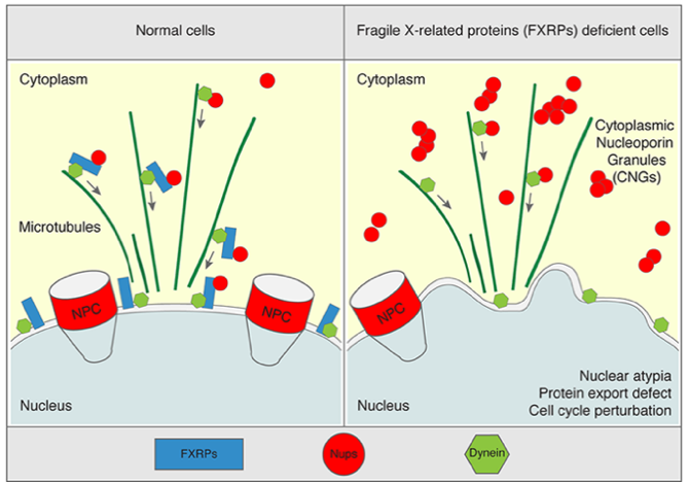
Fig. 2. Un modèle montrant comment les FXRPs contrôlent l'homéostasie des Nups. Les FXRPs (bleu) interagissent avec les Nups solubles cytoplasmiques (cercles rouges) et la dynéine (vert) et facilitent leur localisation dans l’EN au début de la phase G1. La déplétion des FXRPs ou la perturbation du transport le long des microtubules, conduit à l'accumulation des GNC, à des défauts d'exportation des protéines et de la progression du cycle cellulaire, ce qui peut contribuer à la pathologie du SXF. Adapté de Agote-Aran et al, EMBO J 2020.
3. Le rôle de nouvelles protéines de liaison à l'ubiquitine pendant la sortie de la mitose et l'assemblage des complexes de pores nucléaires
En recherchant de nouvelles protéines de liaison à l'ubiquitine régulant la division cellulaire, nous avons identifié NICE4/UBAP2L comme un facteur important pour la bonne exécution de la sortie mitotique. Nous avons pu démontrer que NICE4 régule la fidélité de la sortie mitotique et la reformation de l'enveloppe nucléaire (EN) à la fin de la mitose. En effet, l'inactivation de NICE4 dans les cellules humaines entraîne des noyaux polylobés de forme irrégulière et des défauts dans l'assemblage des nucléoporines.
L'analyse de la spectrométrie de masse a identifié la famille Fragile-X (FXR) comme interagissant avec NICE4/UBAP2L, ce qui suggère que NICE4/UBAP2L pourrait être impliqué dans la régulation de la voie d'assemblage des Nups. En effet, NICE4/UBAP2L interagit fortement avec FXR1 et FRMP et les cellules knock-out CRISPR/Cas9 pour NICE4/UBAP2L présentent la même condensation de Nups et les mêmes défauts nucléaires que les cellules déficientes en FXRPs. La déplétion de NICE4/UBAP2L peut également inhiber la localisation des FXRPs à l'enveloppe nucléaire et conduit à l'agrégation cytoplasmique des FXRPs, ce qui suggère que NICE4/UBAP2L régule spatialement leur fonction et agit comme un chaperon pour la localisation cellulaire correcte des FXRPs. Il est intéressant de noter que la fonction de NICE4/UBAP2L en tant que chaperon pour les FXRPs est exclusivement médiée par son domaine RGG situé dans la partie N-terminale de la protéine.Le domaine RGG est suffisant pour interagir avec les FXRPs, suggérant que NICE4/UBAP2L régule les FXRPs d'une manière indépendante de l'ubiquitine. Il reste à étudier comment exactement NICE4/UBAP2L contribue à la régulation de l'assemblage des FXRPs au niveau de l'enveloppe nucléaire et à la prolifération cellulaire et comment des défauts dans cette voie peuvent contribuer à des maladies humaines telles que le cancer et le syndrome du X fragile.
En outre, nous cherchons à identifier les cibles de NICE4/UBAP2L, qui pourraient être reconnues de manière dépendante de l'ubiquitine et contribuer à la régulation de la fidélité de la sortie mitotique. Nos activités futures à long terme se concentreront également sur l'identification d'autres protéines de liaison à l'ubiquitine cruciales requises pour la progression du cycle cellulaire.
Publications
2024
Pré-publication, Document de travail
Annulate Lamellae biogenesis is essential for nuclear pore function
- Junyan Lin
- Arantxa Agote-Arán
- Yongrong Liao
- Rafael Schoch
- Paolo Ronchi
- Victor Cochard
- Rui Zhu
- Charlotte Kleiss
- M. Ruff
- Guillaume Chevreux
- Yannick Schwab
- Bruno P. Klaholz
- Izabela Sumara
Article dans une revue
Cytoplasmic nucleoporin assemblage: the cellular artwork in physiology and disease
- Junyan Lin
- Izabela Sumara
Nucleus ; Volume: 15 ; Page: 2387534
Article dans une revue
UBAP2L ensures homeostasis of nuclear pore complexes at the intact nuclear envelope
- Yongrong Liao
- Leonid Andronov
- Xiaotian Liu
- Junyan Lin
- Lucile Guerber
- Linjie Lu
- Arantxa Agote-Arán
- Evanthia Pangou
- Li Ran
- Charlotte Kleiss
- Mengdi Qu
- Stephane Schmucker
- Luca Cirillo
- Zhirong Zhang
- Daniel Riveline
- Monica Gotta
- Bruno P Klaholz
- Izabela Sumara
Journal of Cell Biology ; Volume: 223 ; Page: e202310006
2023
Article dans une revue
UBAP2L ‐dependent coupling of PLK1 localization and stability during mitosis
- Lucile Guerber
- Aurore Vuidel
- Yongrong Liao
- Charlotte Kleiss
- Erwan Grandgirard
- Izabela Sumara
- Evanthia Pangou
EMBO Reports ; Volume: 24
Article dans une revue
CaMK1D signalling in AgRP neurons promotes ghrelin-mediated food intake
- Karl Vivot
- Gergo Meszaros
- Evanthia Pangou
- Zhirong Zhang
- Mengdi Qu
- Eric Erbs
- Gagik Yeghiazaryan
- Mar Quiñones
- Erwan Grandgirard
- Anna Schneider
- Etienne Clauss-Creusot
- Alexandre Charlet
- Maya Faour
- Claire Martin
- Fedor Berditchevski
- Izabela Sumara
- Serge Luquet
- Peter Kloppenburg
- Rubén Nogueiras
- Roméo Ricci
Nature Metabolism ; Volume: 5 ; Page: 1045-1058
Article dans une revue
KCNN4 links PIEZO-dependent mechanotransduction to NLRP3 inflammasome activation
- Li Ran
- Tao Ye
- Eric Erbs
- Izabela Sumara
- Romeo Ricci
- Zhirong Zhang
- Stephan Ehl
- Nathalie Spassky
Science Immunology ; Volume: 8 ; Page: adf4699
2022
Article dans une revue
Non-proteolytic ubiquitylation in cellular signaling and human disease
- Yongrong Liao
- Izabela Sumara
- Evanthia Pangou
Communications Biology ; Volume: 5 ; Page: 114
Pré-publication, Document de travail
UBAP2L-dependent coupling of PLK1 localization and stability during mitosis
- Lucile Guerber
- Evanthia Pangou
- Aurore Vuidel
- Yongrong Liao
- Charlotte Kleiss
- Erwan Grandgirard
- Izabela Sumara
Article dans une revue
Phosphorylation of XPD drives its mitotic role independently of its DNA repair and transcription functions
- Emmanuel Compe
- Evanthia Pangou
- Nicolas Le May
- Clémence Elly
- Cathy Braun
- Ji-Hyun Hwang
- Frédéric Coin
- Izabela Sumara
- Kwang-Wook Choi
- Jean-Marc Egly
Science Advances ; Volume: 8
Article dans une revue
Ubiquitin Binding Protein 2-Like (UBAP2L): is it so NICE After All?
- Lucile Guerber
- Evanthia Pangou
- Izabela Sumara
Frontiers in Cell and Developmental Biology ; Volume: 10
Page 1 sur 4
Collaborations et réseaux
- Kay Hofmann (University of Cologne, Germany)
- Radislav Sedlacek (University of Prag, Czech Republic)
- Pascal Villa (PCBIS, Illkirch France)
- Dominique Bonnet (University of Strasbourg, France)
- Karim Hnia (I2MC, Toulouse, France)
- Julien Vermot (Imperial College London, London, UK)
- Valerie Doye (IJM, Paris , France)
- Claudia Bagni (University of Lausanne, Switzerland)
- Yannick Schwab (EMBL Heidelberg, Germany)
- Romeo Ricci (IGBMC, Illkirch, France)
- Catherine Tomasetto (IGBMC, Illkirch, France)
- Jamel Chelly (IGBMC, Illkirch, France)
- Hervé Moine (IGBMC, Illkirch, France)
- Jean-Louis Mandel (IGBMC, Illkirch, France)
- Bruno Klaholz (IGBMC, Illkirch, France)
Prix/Distinctions
- Prime d’Excellence Scientifique from CNRS, 2011-2014, 2016-2020
- University of Strasbourg Institute for Advanced Study (USIAS) 2014
- Sanofi Innovation Awards Program Europe (iAwards) 2018
Financements et partenaires
- ATIP-Avenir Research Grant (R10076MS) 2010
- “Programme de Mécénat“ with Sanofi Aventis and Aviesan 2010
- La Ligue Contre le Cancer 2013, 2014, 2015, 2020
- University of Strasbourg Institute for Advanced Study (USIAS) 2014
- SATT Conectus Alsace 2015, 2019
- Fondation ARC pour la recherche sur le cancer - Programme Labellisé Fondation ARC pour la recherche sur le cancer 2016
- L'Institut National du Cancer (INCa) 2016 - Projets libres de Recherche Biologie et Sciences du Cancer 2016
- Agence Nationale de la Recherche (ANR) AAPG project 2017
- Sanofi Innovation Awards Program Europe (iAwards) 2018
- Programme Fédérateur Aviesan: Vers une nouvelle carte subcellulaire de la cellule cancéreuse, 2019 Plan Cancer 2019

