Différenciation et physiopathologie des cellules endocrines pancréatiques et intestinales
Différenciation et physiopathologie des cellules endocrines pancréatiques et intestinales
Notre objectif principal est d’élucider les réseaux de régulation transcriptionelle qui contrôlent la différenciation, la fonction et le maintien de l’identité des cellules endocrines du pancréas et de l’intestin et d’étudier leurs dysfonctionnements dans les maladies métaboliques comme le diabète.
Les stratégies futures de thérapie cellulaire et de médecine régénérative dépendent fortement de la connaissance détaillée des mécanismes de différenciation des cellules souches multipotentes en cellules hautement spécialisées. Dans ce contexte, notre but est de comprendre comment les cellules endocrines du pancréas et de l’intestin sont générées à partir des cellules souches/progénitrices durant l’embryogénèse et jusqu’à la vie adulte.
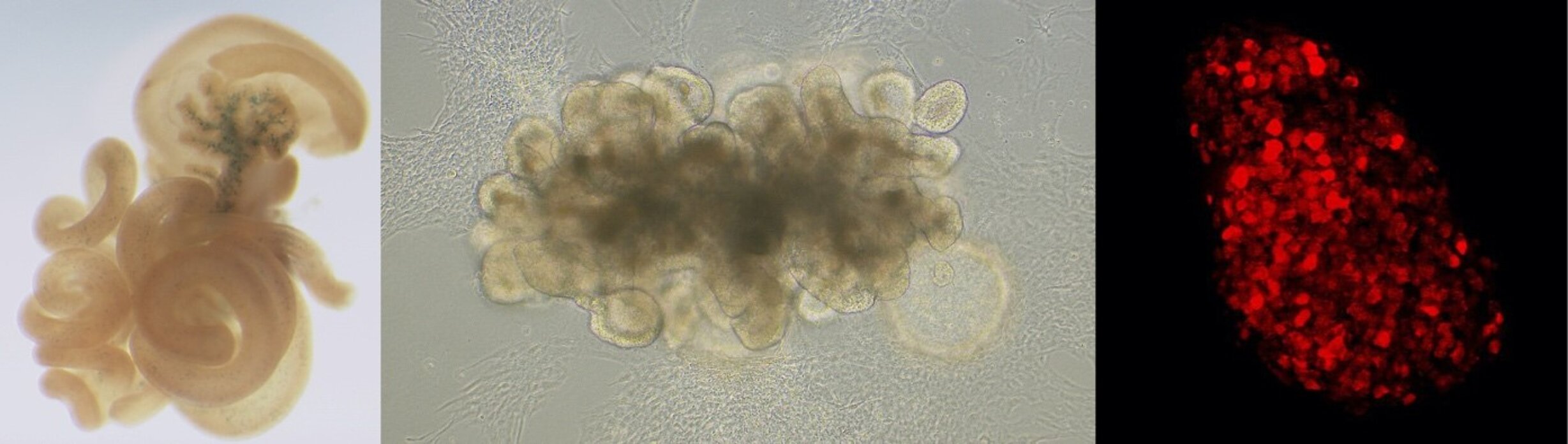
Les cellules endocrines pancréatiques sont regroupées en îlots au sein du tissu exocrine. Ces îlots comprennent cinq types de cellules endocrines produisant des hormones différentes, dont les cellules bêta sécrétrices d'insuline. Ces hormones contrôlent de concert l’homéostasie du glucose. La destruction des cellules bêta ou leur dysfonctionnement conduit au diabète. Les cellules endocrines intestinales, également appelées cellules entéroendocrines (CEE), sont très étroitement liées aux cellules endocrines pancréatiques en ce qui concerne leur origine embryonnaire, leurs programmes de différenciation et leurs rôles physiologiques dans le contrôle de l'homéostasie énergétique. Les CEEs sont des cellules rares de la muqueuse intestinale, elles détectent les nutriments dans la lumière intestinale et, en réponse, sécrètent une variété d'hormones qui agissent localement ou à distance pour réguler l'homéostasie énergétique via leur contrôle de l'absorption intestinale, de la prise alimentaire et de la sécrétion d'insuline. Nous avons montré précédemment, qu’à la fois dans le pancréas et l’intestin, l’ensemble des cellules endocrines dérivent de cellules progénitrices exprimant le facteur de transcription pro-endocrinien Neurog3. En l'absence de Neurog3, les cellules des îlots de Langerhans et les CEEs ne se forment pas, entraînant un diabète néonatal et une malabsorption intestinale chez la souris et l'homme. Malgré la fonction essentielle de ce facteur de transcription et l'identification de quelques gène cibles de Neurog3, les mécanismes moléculaires mettant en œuvre la fonction endocrinogénique de Neurog3 sont mal compris.
Dans ce contexte, nous nous concentrons sur l'identification et l'étude de nouveaux gènes contrôlant la spécification et la spécialisation des sous-types cellulaires endocrines et leur maturation fonctionnelle. Pour répondre à ces questions, nous utilisons des systèmes de culture d'organoïdes humains dérivés de cellules souches et des modèles murins combinés à des approches de perte de fonction et multi-omiques. Nous espérons que nos études contribueront au développement d'une thérapie cellulaire du diabète, ainsi qu'à comprendre les mécanismes sous-jacents des insuffisances endocriniennes pancréatiques et intestinales chez l'homme.

Membres
Chercheur(euse)s
Doctorant(e)s
Ingénieur(eure)s
Technicien(ne)s
Financements et partenaires
L’équipe a été soutenue par des financements de
- Novonordisk Foundation
- Agence National pour la Recherche (ANR)
- Fondation pour la Recherche Médicale (FRM)
- Novonordisk
- National Institute for Diabetes and Digestive and Kidney Disease (NIDDK)
- Société Francophone du Diabète (SFD)
- Juvenile Diabetes Research Foundation (JDRF)
- Union Européenne (6th FP)
- Institut Benjamin Delessert
- Association Française des Diabétiques (AFD)
- Université de Strasbourg
- ARC
- INSERM-AVENIR
Actualités
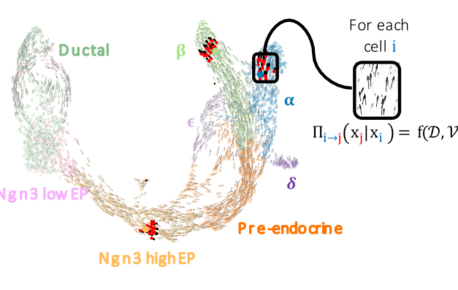
FateCompass : identifier et prédire les critères décisifs du destin cellulaire
La différenciation cellulaire est un processus régulé par l’expression des gènes grâce à l’action de facteurs de transcription. Différents facteurs de…
Lire la suite
Ressources
Organoïde intestinal humain. Les progéniteurs entéroendocrines expriment le facteur de transcription NEUROG3 (rouge).
Publications
2008
Article dans une revue
Characterization of the proneural gene regulatory network during mouse telencephalon development
- Julia M. Gohlke
- Olivier Armant
- Frederick M. Parham
- Marjolein V. Smith
- Celine Zimmer
- Diogo S. Castro
- Laurent Nguyen
- Joel S. Parker
- Gerard Gradwohl
- Christopher J. Portier
- François Guillemot
BMC Biology ; Volume: 6
Article dans une revue
The macroPARP genes Parp-9 and Parp-14 are developmentally and differentially regulated in mouse tissues.
- Antoinette Hakmé
- Aline Huber
- Pascal Dollé
- Valérie Schreiber
Developmental Dynamics ; Volume: 237 ; Page: 209-15
Article dans une revue
β Cells Can Be Generated from Endogenous Progenitors in Injured Adult Mouse Pancreas
- Xiaobo Xu
- Joke d'Hoker
- Geert Stangé
- Stefan Bonné
- Nico de Leu
- Xiangwei Xiao
- Mark van de Casteele
- Georg Mellitzer
- Zhidong Ling
- Danny Pipeleers
- Luc Bouwens
- Raphael Scharfmann
- Gerard Gradwohl
- Harry Heimberg
Cell ; Volume: 132 ; Page: 197-207
Article dans une revue
GeneSpeed Beta Cell: an online genomics data repository and analysis resource tailored for the islet cell biologist
- Nayeem Quayum
- Alecksandr Kutchma
- Suparna A. Sarkar
- Kirstine Juhl
- Gerard Gradwohl
- Georg Mellitzer
- John C. Hutton
- Jan Jensen
Experimental Diabetes Research ; Volume: 2008
2007
Article dans une revue
PARP-2 controls adipocyte differentiation and adipose tissue function through the regulation of the activity of the RXR/PPARgamma heterodimer.
- Péter Bai
- Sander M Houten
- Aline Huber
- Valérie Schreiber
- Mitsuhiro Watanabe
- Borbála Kiss
- Gilbert de Murcia
- Johan Auwerx
- Josiane Ménissier-de Murcia
Journal of Biological Chemistry ; Page: epub ahead of print
Article dans une revue
Neuronal expression of muskelin in the rodent central nervous system.
- Nadia Tagnaouti
- Sven Loebrich
- Frank Heisler
- Yvonne Pechmann
- Susanne Fehr
- Adèle de Arcangelis
- Elisabeth Georges-Labouesse
- Josephine C Adams
- Matthias Kneussel
BMC Neuroscience ; Volume: 8 ; Page: 28
Article dans une revue
Regulation of post-translational modifications of muskelin by protein kinase C.
- Soren Prag
- Adèle de Arcangelis
- Elisabeth Georges-Labouesse
- Josephine C Adams
International Journal of Biochemistry and Cell Biology ; Volume: 39 ; Page: 366-78
2006
Article dans une revue
Basement membrane attachment is dispensable for radial glial cell fate and for proliferation, but affects positioning of neuronal subtypes.
- Nicole Haubst
- Elisabeth Georges-Labouesse
- Adèle de Arcangelis
- Ulrike Mayer
- Magdalena Götz
Development (Cambridge, England) ; Volume: 133 ; Page: 3245-54
2005
Article dans une revue
Genetic determinants of pancreatic epsilon-cell development.
- R Scott Heller
- Marjorie Jenny
- Patrick Collombat
- Ahmed Mansouri
- Catherine Tomasetto
- Ole D Madsen
- Georg Mellitzer
- Gerard Gradwohl
- Palle Serup
Developmental Biology ; Volume: 286 ; Page: 217-24
Article dans une revue
Genetic determinants of pancreatic ε-cell development
- R. Scott Heller
- Marjorie Jenny
- Patrick Collombat
- Ahmed Mansouri
- Catherine Tomasetto
- Ole Madsen
- Georg Mellitzer
- Gerard Gradwohl
- Palle Serup
Developmental Biology ; Volume: 286 ; Page: 217-224

