Différenciation et physiopathologie des cellules endocrines pancréatiques et intestinales
Différenciation et physiopathologie des cellules endocrines pancréatiques et intestinales
Notre objectif principal est d’élucider les réseaux de régulation transcriptionelle qui contrôlent la différenciation, la fonction et le maintien de l’identité des cellules endocrines du pancréas et de l’intestin et d’étudier leurs dysfonctionnements dans les maladies métaboliques comme le diabète.
Les stratégies futures de thérapie cellulaire et de médecine régénérative dépendent fortement de la connaissance détaillée des mécanismes de différenciation des cellules souches multipotentes en cellules hautement spécialisées. Dans ce contexte, notre but est de comprendre comment les cellules endocrines du pancréas et de l’intestin sont générées à partir des cellules souches/progénitrices durant l’embryogénèse et jusqu’à la vie adulte.
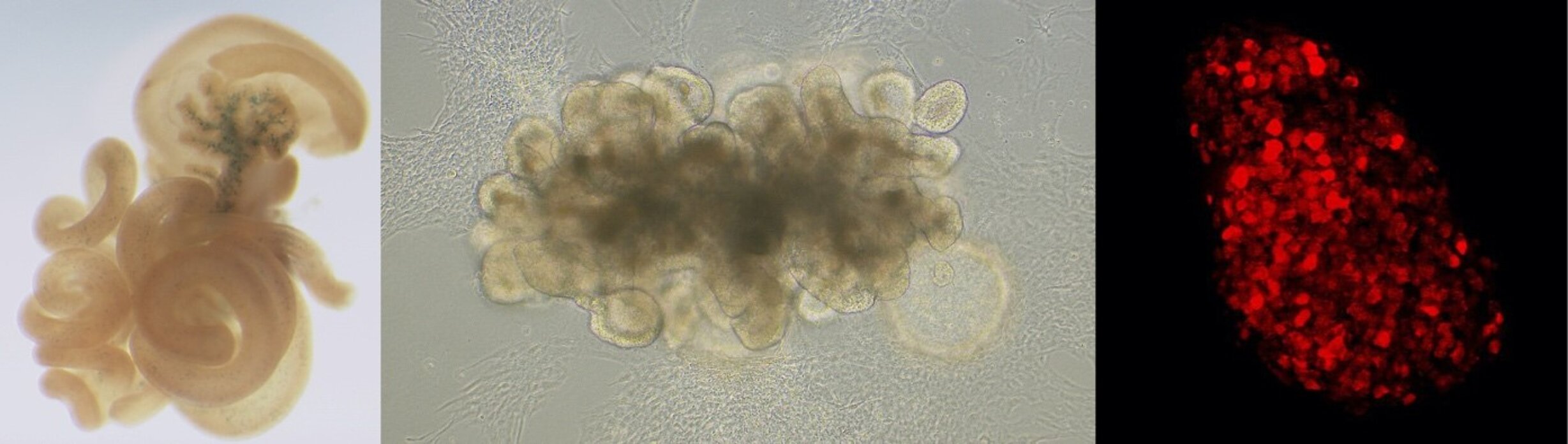
Les cellules endocrines pancréatiques sont regroupées en îlots au sein du tissu exocrine. Ces îlots comprennent cinq types de cellules endocrines produisant des hormones différentes, dont les cellules bêta sécrétrices d'insuline. Ces hormones contrôlent de concert l’homéostasie du glucose. La destruction des cellules bêta ou leur dysfonctionnement conduit au diabète. Les cellules endocrines intestinales, également appelées cellules entéroendocrines (CEE), sont très étroitement liées aux cellules endocrines pancréatiques en ce qui concerne leur origine embryonnaire, leurs programmes de différenciation et leurs rôles physiologiques dans le contrôle de l'homéostasie énergétique. Les CEEs sont des cellules rares de la muqueuse intestinale, elles détectent les nutriments dans la lumière intestinale et, en réponse, sécrètent une variété d'hormones qui agissent localement ou à distance pour réguler l'homéostasie énergétique via leur contrôle de l'absorption intestinale, de la prise alimentaire et de la sécrétion d'insuline. Nous avons montré précédemment, qu’à la fois dans le pancréas et l’intestin, l’ensemble des cellules endocrines dérivent de cellules progénitrices exprimant le facteur de transcription pro-endocrinien Neurog3. En l'absence de Neurog3, les cellules des îlots de Langerhans et les CEEs ne se forment pas, entraînant un diabète néonatal et une malabsorption intestinale chez la souris et l'homme. Malgré la fonction essentielle de ce facteur de transcription et l'identification de quelques gène cibles de Neurog3, les mécanismes moléculaires mettant en œuvre la fonction endocrinogénique de Neurog3 sont mal compris.
Dans ce contexte, nous nous concentrons sur l'identification et l'étude de nouveaux gènes contrôlant la spécification et la spécialisation des sous-types cellulaires endocrines et leur maturation fonctionnelle. Pour répondre à ces questions, nous utilisons des systèmes de culture d'organoïdes humains dérivés de cellules souches et des modèles murins combinés à des approches de perte de fonction et multi-omiques. Nous espérons que nos études contribueront au développement d'une thérapie cellulaire du diabète, ainsi qu'à comprendre les mécanismes sous-jacents des insuffisances endocriniennes pancréatiques et intestinales chez l'homme.
.png)
Membres
Chercheur(euse)s
Doctorant(e)s
Technicien(ne)s
Financements et partenaires
L’équipe a été soutenue par des financements de
- Novonordisk Foundation
- Agence National pour la Recherche (ANR)
- Fondation pour la Recherche Médicale (FRM)
- Novonordisk
- National Institute for Diabetes and Digestive and Kidney Disease (NIDDK)
- Société Française des Diabétiques (SFD)
- Juvenile Diabetes Research Foundation (JDRF)
- Union Européenne (6th FP)
- Institut Benjamin Delessert
- Association Française des Diabétiques (AFD)
- Université de Strasbourg
- ARC
- INSERM-AVENIR
Actualités
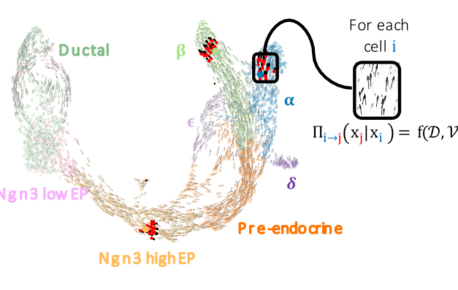
FateCompass : identifier et prédire les critères décisifs du destin cellulaire
La différenciation cellulaire est un processus régulé par l’expression des gènes grâce à l’action de facteurs de transcription. Différents facteurs de…
Lire la suite
Ressources
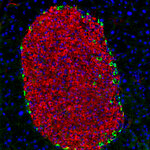
Organoïde intestinal humain. Les progéniteurs entéroendocrines expriment le facteur de transcription NEUROG3 (rouge).
Publications
-
2003
-
Opposing actions of Arx and Pax4 in endocrine pancreas development
- Patrick Collombat
- Ahmed Mansouri
- Jacob Hecksher-Sorensen
- Palle Serup
- Jens Krull
- Gerard Gradwohl
- Peter Gruss
Genes and Development ; Volume: 17 ; Page: 2591-2603
-
Transcriptional program of the endocrine pancreas in mice and humans
- Klaus H. Kaestner
- Catherine S. Lee
- L. Marie Scearce
- John E. Brestelli
- Athanasios Arsenlis
- Phillip Phuc Le
- Kristen A. Lantz
- Jonathan Crabtree
- Angel Pizarro
- Joan Mazzarelli
- Deborah Pinney
- Steve Fischer
- Elisabetta Manduchi
- Christian J. Stoeckert
- Gerard Gradwohl
- Sandra W. Clifton
- Juliana R. Brown
- Hiroshi Inoue
- Corentin Cras-Méneur
- M. Alan Permutt
Diabetes ; Volume: 52 ; Page: 1604-1610
-
-
2002
-
Neurogenin3 is differentially required for endocrine cell fate specification in the intestinal and gastric epithelium
- Marjorie Jenny
- Céline Uhl
- Colette Roche
- Isabelle Duluc
- Valérie Guillermin
- Francois Guillemot
- Jan Jensen
- Michèle Kedinger
- Gerard Gradwohl
The EMBO Journal ; Volume: 21 ; Page: 6338-6347
-
-
2001
-
Crossregulation between Neurogenin2 and pathways specifying neuronal identity in the spinal cord
- Raffaella Scardigli
- Carol Schuurmans
- Gerard Gradwohl
- François Guillemot
Neuron ; Volume: 31 ; Page: 203-217
-
-
2000
-
Transcription Factor Hepatocyte Nuclear Factor 6 Regulates Pancreatic Endocrine Cell Differentiation and Controls Expression of the Proendocrine Gene <i>ngn3</i>
- Patrick Jacquemin
- Serge M. Durviaux
- Jan Jensen
- Catherine Godfraind
- Gerard Gradwohl
- François Guillemot
- Ole D. Madsen
- Peter Carmeliet
- Mieke Dewerchin
- Désiré Collen
- Guy G. Rousseau
- Frédéric P. Lemaigre
Molecular and cellular biology ; Volume: 20 ; Page: 4445-4454
-
neurogenin3 is required for the development of the four endocrine cell lineages of the pancreas
- Gérard Gradwohl
- Andrée Dierich
- Marianne Lemeur
- François Guillemot
Proceedings of the National Academy of Sciences of the United States of America ; Volume: 97 ; Page: 1607-1611
-
-
1999
-
Hes1 and Hes5 as notch effectors in mammalian neuronal differentiation
- Toshiyuki Ohtsuka
- Makoto Ishibashi
- Gerard Gradwohl
- Shigetada Nakanishi
- François Guillemot
- Ryoichiro Kageyama
EMBO Journal ; Volume: 18 ; Page: 2196-2207
-
-
1998
-
The bHLH Protein NEUROGENIN 2 Is a Determination Factor for Epibranchial Placode–Derived Sensory Neurons
- Carol Fode
- Gérard Gradwohl
- Xavier Morin
- Andrée Dierich
- Marianne Lemeur
- Christo Goridis
- François Guillemot
Neuron ; Volume: 20 ; Page: 483-494
-
-
1997
-
The activity of neurogenin1 is controlled by local cues in the zebrafish embryo
- P Blader
- Natacha Schroeder
- Gerard Gradwohl
- F Guillemot
- U Strähle
Development (Cambridge, England) ; Volume: 124 ; Page: 4557-4569
-
-
1996
-
Restricted Expression of a Novel Murineatonal-Related bHLH Protein in Undifferentiated Neural Precursors
- Gérard Gradwohl
- Carol Fode
- François Guillemot
Developmental Biology ; Volume: 180 ; Page: 227-241
-
Page 4 sur 4

